点击图片,立即报名
2021年6月17日/医麦客新闻 eMedClub News/--近日,Autolus Therapeutics plc宣布AUTO1(obe-cel)已获得英国药品和保健品监管局(MHRA)关于创新许可和获取途径(ILAP),该CAR-T细胞疗法用于FELIX1b/2期复发/难治性(r/r),正在研究成人B细胞急性淋巴细胞白血病(ALL)。

ILAP于2020年12月宣布并于2021年初推出,旨在加速开发和获得有前景的药物,主要面向处于早期开发阶段的药物。该途径是英国在脱欧后吸引生命科学发展计划的一部分,其特点是加强了与MHRA和其他利益相关者的投入和互动,其中包括国家健康与护理卓越研究所(NICE)和苏格兰药物联盟(SMC)。
创新护照认定是ILAP流程的第一步,并触发MHRA及其合作机构为监管和发展里程碑制定路线图,目标是在英国实现早期患者准入。ILAP的其他好处包括访问一系列开发工具,例如150天加速营销授权申请(MAA)评估、滚动审查和持续收益风险评估的机会。
“ILAP对obe-cel的指定,以及最近欧洲药品管理局(EMA)的优先医学(PRIME)相关认定,是加速这种有前景疗法的审查过程的又一步,”Autolus首席执行官Christian Itin博士对奥托卢斯的官员说,“Obe-cel在功效、耐久性和安全性方面不断显示出与其他CAR-T细胞产品不同的潜力,并且可以通过为r/r ALL提供潜在的治愈性疗法来改变护理标准。”
▲Autolus首席执行官Christian Itin博士 (图片来源:biozentrum.unibas.ch)
AUTO1是以CD19为靶点的T细胞疗法,被设计为具有快速结合动力学的CD19,允许CAR-T细胞有效识别癌细胞,并注射细胞毒性蛋白启动细胞自我破坏过程、快速解离,然后再去结合下一个癌细胞。这个过程也被称为“连环杀手”。相比较于传统的anti-CD19 CAR-T细胞疗法,AUTO1具有相同的结合率和更快的解离率。使得其能够在保持相似水平疗效的同时,提供更高的安全性。
AUTO1在儿童急性B细胞白血病患者中的高CR率与优异的持久性、安全性已经获得临床试验的肯定。目前正在两项1期研究中进行评估,一项用于复发/难治性成人急性淋巴细胞白血病,一项用于成人复发/难治性惰性B细胞淋巴瘤。该公司现在还将该计划推进到一项潜在的关键研究AUTO1-AL1。
AUTO1-AL1研究将招募复发/难治性ALL患者。在进行2期研究之前,该研究将有一个简短的1b阶段。主要终点是总体反应率,关键次要终点包括反应持续时间、MRD阴性CR率和安全性。该研究将在美国、英国和欧洲的30个领先的学术和非学术中心招募约100名患者。
6月11日,Autolus在2021年欧洲血液学协会(EHA)虚拟大会上更新了r/r成人急性淋巴细胞白血病(ALL)患者的反应持续时间。会议上提供的早期数据表明obe-cel作为独立疗法对一些成人ALL患者同样具有治愈潜力。
AUTO1在不同队列中的结果反馈
复发/难治性惰性B细胞淋巴瘤
截至数据截止日期2021年5月17日,D队列中共有9名可研究的r/r IBCL患者,所有接受治疗的患者都实现了完全缓解,且数据显示Obe-cel耐受性良好,在r/r低级别B细胞淋巴瘤成人患者中表现出良好的安全性。
安全性报告显示4名患者发生1级CRS,1名患者发生了2级CRS。且未观察到任何级别的免疫效应细胞相关神经毒性综合征(ICANS)。
在中位随访6个月中,9名患者中有8名在最后一次随访时无病,1名患者在第6个月复发但通过放疗获救。另有一名患者完全缓解但仍死于COVID-19感染。
复发/难治性成人急性淋巴细胞白血病
截至数据截止日期2021年5月17日,A队列中的20名r/r ALL患者已接受输注obe-cel。结果显示该疗法耐受性良好,85%患者在一个月内达到最小残留病灶(MRD)阴性完全缓解(CR)。
在可评估疗效的20名患者中,未出现3级或更高级别的CRS。15%有高白血病负担的患者经历了3级ICANS,但使用类固醇后迅速缓解。值得注意的是,在所有接受治疗的患者中,患者的无事件生存率(EFS)在接受治疗24个月时为50.2%,而且这一数值在接受治疗12月后一直处于稳定状态。
Autolus是一家临床阶段的生物制药公司,致力于开发用于治疗癌症的下一代程序化T细胞疗法。该公司使用一套广泛的专有和模块化T细胞编程技术,正在设计精确靶向、受控和高活性的T细胞疗法,旨在更好地识别癌细胞、分解其防御机制并消除这些细胞。Autolus拥有一系列正在开发的候选产品,用于治疗血液系统恶性肿瘤和实体瘤。
靶向CD19的CAR-T细胞疗法AUTO1,是Autolus公司第一个进入后期开发阶段的候选产品。目前正处于多个适应症的1/2期临床试验中,包括成人/儿童急性淋巴细胞白血病(ALL)、惰性非霍奇金淋巴瘤(iNHL)、慢性淋巴细胞白血病(CLL)以及原发性中枢神经系统淋巴瘤(PCNSL)。
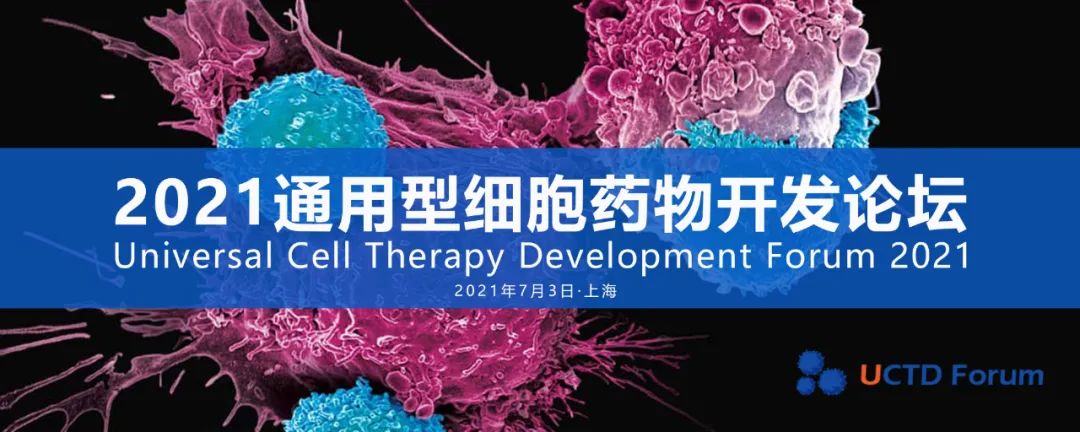
▲处于临床阶段的项目管道(图片来源:autolus)
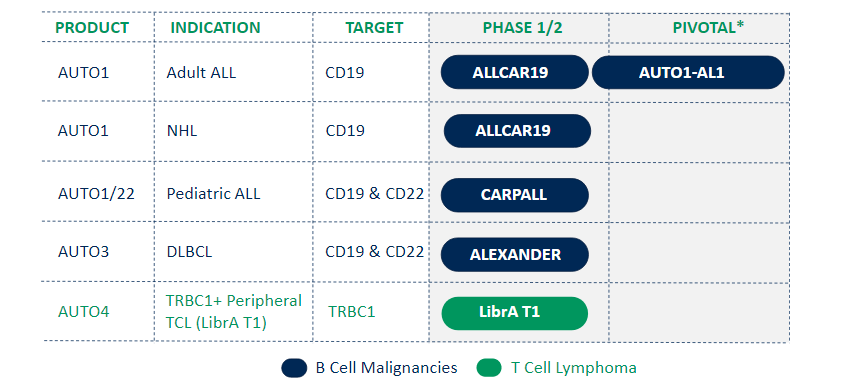
▲处于临床前阶段的项目管道(图片来源:autolus)
CAR-T领域的竞争也日渐激烈,能够在该领域占据一席之地的必然是具备核心竞争力的CAR-T企业。
在此,我们也期待着Autolus公司CAR-T疗法的新思路能够在接下来的临床试验中得到有力的验证,为广大癌症患者带来更有效、更安全、更具成本效益的治疗方案。
参考资料:
1.https://autolus.gcs-web.com/news-releases/news-release-details/autolus-therapeutics-announces-innovation-licensing-and-access
医麦客始终致力于生物创新药的前沿技术、行业动态、产业洞察等原创新闻报道,全媒体高端矩阵用户达16万+,其中工业用户占比超50%,科研与临床用户约为30%,投资机构用户超过5%。为促进产业细分领域的互动交流,我们组建了多个专业微信群,欢迎扫码加群。