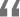2020年3月10日/医麦客新闻 eMedClub News/--3月6日,英国癌症基因治疗公司PsiOxus Therapeutics宣布,公司已开始对癌症患者进行NG-641的临床试验,这是一项四种转基因修饰肿瘤微环境的癌症基因治疗,是该公司第三个进入临床评估的癌症基因疗法。同时,这也是首次将一种含有四种不同治疗转基因的肿瘤特异性病毒应用于癌症患者。

“对于NG-641,我们的方法是系统地传递基因治疗载体,将肿瘤细胞转化为药物工厂,传递一种双特异性T细胞激活蛋白,通过成纤维细胞激活蛋白(FAP)靶向与癌症相关的纤维母细胞(cancer-associated fibroblasts,CAFs)。”这种机制使我们能够瞄准肿瘤微环境中最重要的免疫抑制细胞之一,”PsiOxus的首席科学官Brian Champion博士说。
除了 FAP靶向的T细胞激活剂外,NG-641还传递另外三种分子来进一步募集和激活T细胞,从而诱导抗肿瘤免疫反应。因此NG-641是第一个在患者身上研究的四价病毒基因治疗载体。
第一阶段的STAR研究(NCT04053283)正在美国多个癌症中心进行,将评估NG-641在实体瘤患者中的安全性、耐受性和初步抗肿瘤活性。
专利的T-SIGn技术平台
PsiOxus拥有专利的T-SIGn技术平台,该平台使用Enadenotucirev(EnAd)溶瘤病毒作为载体,将治疗性转基因组合递送到实体瘤内,以对抗癌症。
Enadenotucirev是一种非自然产生的B群腺病毒,它是利用定向进化原理产生的一种具有杀灭肿瘤活性和血液稳定性的病毒,因此它允许静脉给药。另外Enadenotucirev还只在肿瘤组织中复制,而不在正常的非癌组织中复制。

▲Enadenotucirev:由定向进化发展而来(图片来源于:PsiOxus Therapeutics官网)
目前,Enadenotucirev已经是一种临床阶段的溶瘤病毒疗法,具有广泛的靶向实体肿瘤的潜力。临床研究已经证实,Enadenotucirev可以静脉注射,在原发和转移性肿瘤中都可以到达和复制,而在非癌细胞中没有复制的证据,这使Enadenotucirev具有全身治疗癌症的潜力。静脉滴注的临床证据是Enadenotucirev与其他溶瘤病毒的重要区别。
Enadenotucirev被认为能够破坏肿瘤细胞,同时吸引免疫系统的细胞来驱动抗肿瘤免疫,可能使肿瘤更容易受到其他治疗的影响,包括化疗和免疫治疗。目前正在美国和欧洲进行临床研究,OCTAVE研究是联合Enadenotucirev和紫杉醇治疗晚期卵巢癌;SPICE研究是与百时美施贵宝合作,将Enadenotucirev与Opdivo(nivolumab)联合应用于多种实体肿瘤临床试验。
PsiOxus专利的第一代溶瘤病毒Enadenotucirev是该公司下一代溶瘤基因治疗病毒平台----肿瘤特异性免疫基因治疗平台(Tumor-Specific Immuno-Gene Therapy,T-SIGn平台)的基础和载体。多达四个基因可以插入到T-SIGn病毒并提供基因组合的同时表达,T-SIGn病毒通过静脉注射并在体内循环,有可能到达原发和转移性肿瘤组织。实际上,T-SIGn产品被设计成把肿瘤细胞变成“药物工厂”,目标是在高治疗浓度下表达肿瘤中的基因,并避免暴露于非肿瘤细胞。T-SIGn基因治疗产品平台在表达多种类型的基因方面具有广泛的用途。


▲ T-SIGn产品平台分类以及武装的EnAd为局部肿瘤提供免疫治疗
(图片来源于:PsiOxus Therapeutics官网)
(1)抗体:基因编码的单个或组合的抗体或抗体片段。NG-350A,是PsiOxus第一个编码全长抗体的病毒,2019年3月已开始进行患者(实体瘤)给药。
(2)双特异性:基因编码双特异性或多特异性抗体。NG-641,与三个额外的免疫增强基因结合,编码一个双特异性抗体。
(3)膜集成配体:基因编码T细胞结合配体或其他与肿瘤细胞膜结合的配体。NG-348,编码CD3和CD80膜锚定配体。
(4)分泌免疫调节剂:基因编码细胞因子和趋化因子。这方面的研究正在进行中。
基于T-SIGn平台,PsiOxus为实体肿瘤的治疗提供了一个能够同时的、局部表达基因组合的差异化管线。病毒在肿瘤中复制的过程中,这些相同的肿瘤细胞被编码的基因同时引导,产生局部对抗癌症的生物疗法。PsiOxus相信这将导致生物抗癌疗法的局部递送到肿瘤微环境从而治疗癌症。此外,PsiOxus的T-SIGn病毒是在一种产品中提供治疗组合,可能对患者、医生和付款人具有显著的商业优势。


▲PsiOxus公司产品管线(图片来源于:PsiOxus Therapeutics官网)
来自制药巨头百时美施贵宝的青睐
早在2016年6月,百时美施贵宝(BMS)和PsiOxus Therapeutics就达成了一项独家临床评估安全合作协议,评估Opdivo (nivolumab)联合PsiOxus的静脉给药溶瘤腺病毒疗法enadenotucirev治疗晚期癌症患者的安全性、耐受性和初步疗效。百时美施贵宝将向PsiOxus一次性支付1000万美元的预付款,双方共同承担开发成本,PsiOxus负责进行第一阶段的研究。
同年12月,BMS又与PsiOxus就溶瘤腺病毒疗法NG-348签署了全球独家许可协议。BMS向PsiOxus支付5000万美元的预付款,PsiOxus将有资格获得9.36亿美元的开发、监管和销售里程碑,以及净销售的特许权使用费。在PsiOxus完成临床前开发后,BMS全权负责与NG-348相关的全球临床开发和商业化活动。2107年12月,NG-348欧洲临床试验申请获批,PsiOxus公司获得了1500万美元的里程碑付款。
为数不多的全身性给药策略
截至目前,FDA批准的首个同时也是唯一一个溶瘤病毒疗法是Amgen(安进)公司的单纯疱疹病毒T-Vec(Imlygic,I型单纯疱疹病毒),瘤内注射用于黑色素瘤的局部治疗方案。
因此,目前在研的大多数溶瘤病毒也都是采用瘤内注射的给药方式,全身性的静脉注射方案是对溶瘤病毒安全性的一大挑战。PsiOxus和Oncolytics Biotech是为数不多的专注于此的溶瘤病毒公司,并且都取得了不错的进展。
Oncolytics Biotech的专利溶瘤病毒产品Pelareorep(REOLYSIN®),一种静脉注射的呼肠孤病毒,也是备受大型药企青睐的项目。目前为止,Pelareorep已分别协同四大巨头药企的免疫检查点抑制剂药物(Bavencio、Keytruda、Opdivo和Tecentriq)进行测试,显示出与免疫检查点抑制剂的协同作用。2017年11月,阿诺医药通过一项区域授权从Oncolytics获得了Pelareorep在大中华区(包括中国大陆、香港、澳门、台湾)、新加坡和韩国的独家开发及销售权利。
在免疫检查点抑制剂不断被开发,其应用瓶颈逐渐明的背景下,溶瘤病毒基于其能够使“冷”肿瘤变“热”的特性,成为了肿瘤免疫组合治疗的重要组成部分。越来越多的临床证据也表明,溶瘤病毒可以加强肿瘤对免疫调节检查点抑制剂的反应率。T-vec(Imlygic)作为FDA批准的首个溶瘤病毒,进一步的开发中,多项与免疫检查点抑制剂如PD-1单抗Keytruda、CTLA-4单抗Yervoy等联用的临床试验已经给出了令人兴奋的结果。

目前对于Oncolytics而言, 其主要目标是让pelareorep尽快获得监管批准。根据FDA在EOP2会议后的最终建议,Oncolytics公司已获得了特殊试验方案评价(SPA)资格,建议在III期试验之前进行生物标志物的鉴定,单独用药3期研究的确认是得到批准所必须的。
大型药企强势布局溶瘤病毒领域
随着全球肿瘤药物市场预计到2025年将以7.6%的年复合增长率达到1765亿美元,大型制药公司越来越有兴趣利用病毒的力量来对抗癌症。据估计,到2025年,单是治疗性癌症疫苗市场就将超过150亿美元。
在利用病毒对抗癌症的策略中,溶瘤病毒的治疗方法利用各种类型的病毒来刺激患者的免疫系统做出反应,并以更高的效率攻击癌细胞。继Amgen(安进)公司的单纯疱疹病毒Imlygic(T-Vec)后,第二款获FDA批准的溶瘤病毒何时出现,目前仍存在许多未知数,而癌症发病率和患病率上升在内的各项因素又在不断推动市场的增长。
因此,国内外众多制药企业纷纷通过自主研发、技术引进、大量投资等方式来布局于这一极具市场潜力的领域。仅在2018年,该领域就已经与大型制药公司完成了4项总价值超过10亿美元的交易,参与公司包括默沙东(Merck)、勃林格殷格翰(Boehringer Ingelheim)和杨森(Janssen)等。
2019年12月,日本Takeda Pharmaceutical(武田制药)还斥资逾10亿美元布局一个早期的溶瘤病毒项目。这是与加拿大溶瘤病毒公司Turnstone Biologics公司达成的合作协议,旨在利用Turnstone公司专有的牛痘病毒平台来治疗癌症。武田获得与Turnstone共同开发和商业化RIVAL-01的全球独家许可权,并且双方还合作共同开发基于牛痘病毒平台的其他候选产品。而Turnstone还只在动物模型中测试过它的技术,对于何时开始临床试验,公司暂未披露。

国内在溶瘤病毒这一领域的研发实力不可小觑,Imlygic(T-Vec)之前国内也是有两款溶瘤病毒产品曾获批上市,虽然其疗效还未获得国际认可,但也某种程度上证明了国内企业在这一领域的巨大潜力。近年来,国内溶瘤病毒的开发也取得了较大的进展,已经有多项溶瘤病毒产品在国内进入临床实验阶段。

我们希望PsiOxus公司此次临床试验能顺利进行并达到预期结果,同时也期待随着研发策略的发展和完善以及进一步的临床探索,溶瘤病毒的癌症治疗潜力能进一步得到开发,早日出现第二款获批的溶瘤病毒产品,为患者带来更多的治疗选择!
推荐阅读:
参考出处:
1.https://psioxus.com/wp-content/uploads/2020/03/NG641_New-CMO-and-Trial-Start_Press_Release.pdf
2.PsiOxus公司官网